Sonbaharda Yapraklar Neden Renk Değiştirir?

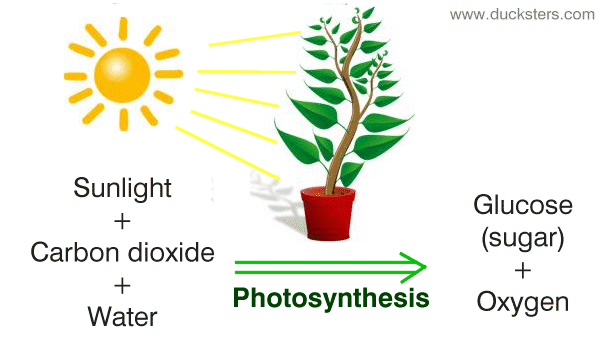
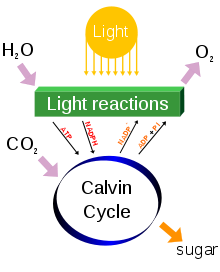
Sonbahar mevsiminin en belirgin özelliklerinden biri doğadaki renk cümbüşüdür. Ağaçların yaprakları yeşilden parlak sarıya, turuncuya, kırmızıya ve kahverengiye doğru renk değiştirir. Ağaçlar da tıpkı bazı hayvanlar gibi ilkbahar ve yaz aylarında bünyelerinde enerji ve besin maddesi depolar ve kış aylarında dinlenme sürecine geçerler. İlkbahar ve yaz aylarında bitkiler ve ağaçlar güneş ışığını fotosentez yaparak enerjiye dönüştürür. Bütün bitkilerin yapısında, renk veren çeşitli pigmentler bulunur. Yapraklara yeşil rengi veren klorofil pigmenti fotosentezin gerçekleşmesini sağlayan kimyasal bir bileşendir. Ancak, sonbahar ve kış aylarında fotosentezin gerçekleşmesi için yeterli ışık ve su bulunmadığından yapraklardaki klorofil seviyesi azalır ve diğer renk pigmentleri açığa çıkmaya başlar. Bunlar; yapraklara sarı rengi veren ksantofil, turuncu rengi veren karotin ve kırmızı rengi veren antosiyanindir. Bütün bu renk pigmentleri tüm yapraklarda sürekli bulunmasına rağmen yeşil rengi veren klorofil baskın durumda olduğu için yapraklar yeşil renktedir ve diğer pigmentler maskelenmiş durumdadır. Havaların soğumasıyla birlikte yaprak içerisindeki klorofiller azalmaya başlayınca, karotinlerin parlak turuncu ve sarı renkleri; daha sonra da yapraklardaki fosfat miktarı azaldıkça antosiyaninlerin kırmızı ve eflatun renkleri yapraklarda hâkim olur. Sonbahar renkleri temel olarak sarı ve kırmızıdan oluşur. Sonbaharın ilerleyen günlerinde bazı sarı yapraklar kahverengiye dönüşür. Bu renk değişiminin ardından ağaçlardaki yaprakların tümü en kısa zamanda dökülür.
ALINTIDIR.
https://bilimgenc.tubitak.gov.tr/makale/sonbaharda-yapraklar-neden-renk-degistirir