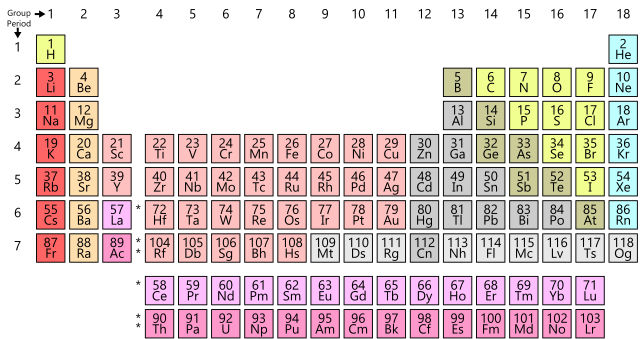
PERİYODİK TABLONUN TARİHÇESİ VE PERİYODİK TABLO
Johann Döberiner: Elementleri fiziksel özelliklerine
göre 3’lü gruplara ayırmıştır.
Periyodik ve Periyodik Tablonun Özellikleri
- Elementler
atom numaralarına göre dizilmiştir.
- Yatay
satırlara periyot, dikey sütunlara grup denir.
- Periyodik
tabloda 8 tane A 10 tane B olmak üzere toplamda 18 grup ve 7 periyot
bulunur.
• Aynı
grupta bulunan elementler benzer kimyasal özellik gösterir.
• Atomların
elektron dizilimindeki katman sayısı periyodu ifade ederken son katmandaki
elektron sayısı grup numarasını verir.
Soldan sağa gidildikçe;
• Grup
numarası artarken periyot sayısı değişmez.
• Atom
numarası artar.
• Benzer
kimyasal özellik azalır.
• Metallik
özellik azalır ametallik özellik artar.
• Periyot numarası artar grup numarası değişmez.
• Atom
numarası artar.
• Benzer
kimyasal özellik artar.
• Ametallik
özellik azalır metal özellik artar.
Elementlerin Sınıflandırılması
Elementler sahip oldukları özelliklere ve kullanım alanlarına
göre 3 grupta incelenir.
Metaller
• Parlak
görünümlüdürler.
• Cıva
hariç hepsi oda sıcaklığında katı halde bulunurlar.
• Şekil
verilirler(tel ve levha haline getirilirler.)
• Elektriği
ve ısıyı iyi iletirler.
• Kendi aralarında bileşik oluşturmazlar. Alaşım denilen homojen karışım oluştururlar.
Yarı Metaller
• Metaller
ile ametaller arasında bulunurlar.
• Parlak
veya mat görünümlü olabilirler.
• Oda
sıcaklığında hepsi katı halde bulunurlar.
• Elektriği
ve ısıyı ametallerden iyi metallerden kötü iletirler.
• İşlenebilirler
Ametaller
• Mat
görünümlüdürler.
• Elektriği
ve ısıyı iyi iletmezler.
• Kırılgandırlar
ve işlenemezler.
• Oda
sıcaklığında katı, sıvı ve gaz halinde bulunabilirler.
• Ametaller
içinde özel bir grup olan soy gazlar yer alır.
Soygazlar
• Oda
sıcaklığında gaz halinde bulunurlar.
• Kararlı
yapıdadırlar, bileşik oluşturmazlar.
• Değerlik
elektron sayısı 2 ve 8’dir.